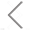血清外泌体追踪COVID-19进展
Author: Mika Huang Date: July 20, 2022
2019年底爆发的冠状病毒(COVID-19)迅速转变为一场全球大流行病,并一直持续至今,对人类健康造成严重和难以预估的长期影响。迄今为止,COVID-19相关的研究主要集中在病毒本身或对其的直接免疫反应上,很少以新冠感染者的外泌体为切入点展开研究。近日来自瑞士苏黎世大学免疫学研究所的Richard Chahwan教授开创性地提出用血清外泌体(EVs)液体活检作为一种新的和独特的方式对COVID-19感染进行诊断和预后分析。文章通过对先天性和获得性免疫EVs分型和SARS-CoV-2 Spike S1阳性EVs等的表征,为COVID-19感染提供了一种新的思路,以追踪受影响的组织和疾病进展的严重程度。
一、研究思路
文章的整体思路是通过收集健康人、早期COVID-19患者(症状出现短于13天)、晚期COVID-19轻症患者(症状出现超过13天)的血液,提取血清中的外泌体,利用nFCM(纳米流式)追踪不同感染天数的外泌体,精确分析患者血液中新冠相关的不同细胞来源的外泌体的大小、颗粒浓度、蛋白表达等,揭示新冠病毒感染人体后,机体内部免疫细胞的应答情况与反应。
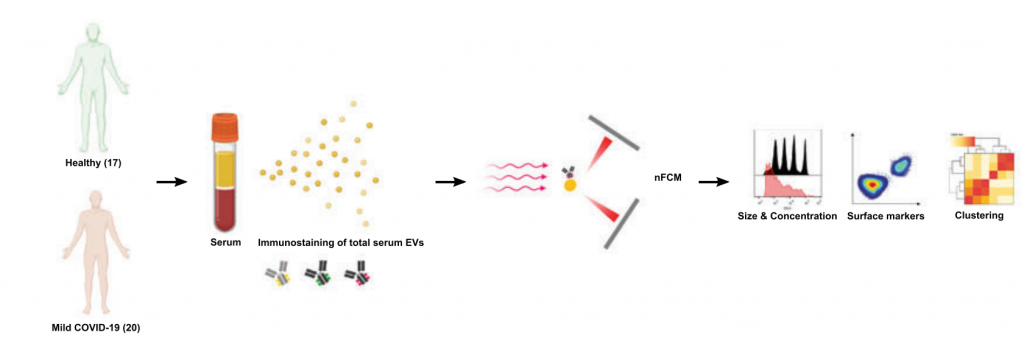
图1 COVID-19外泌体研究示意图
二、新冠患者外泌体表征和亚群分析
根据MISEV2018指南,为了保证结果的重现性,作者对17例健康人和20例轻度新冠感染患者的血清外泌体进行了粒径和浓度等物理性质的表征。从诊断的角度来说,正常人和COVID-19患者血清的EV在不同粒径范围内的差异有望提供有价值的前瞻性信息。根据nFCM的粒径标准品(68, 91, 113, 155 nm)将血清外泌体分成4个不同大小的亚群,分别是small EVs,mild EVs,large EVs和extra large EVs。进一步分析发现新冠患者的外泌体主要集中在small EVs亚群,整体粒径偏小,这与其他学者报道的细胞应激引起较小EVs中度富集相一致。而CD66b阳性的外泌体较健康人有所增加,有趣的是,这种small EVs的富集似乎与extra large EVs (~ 155 nm)的减少相关,并且extra large EVs减少在CD63和CD66b阳性外泌体中更为显著(图2)。
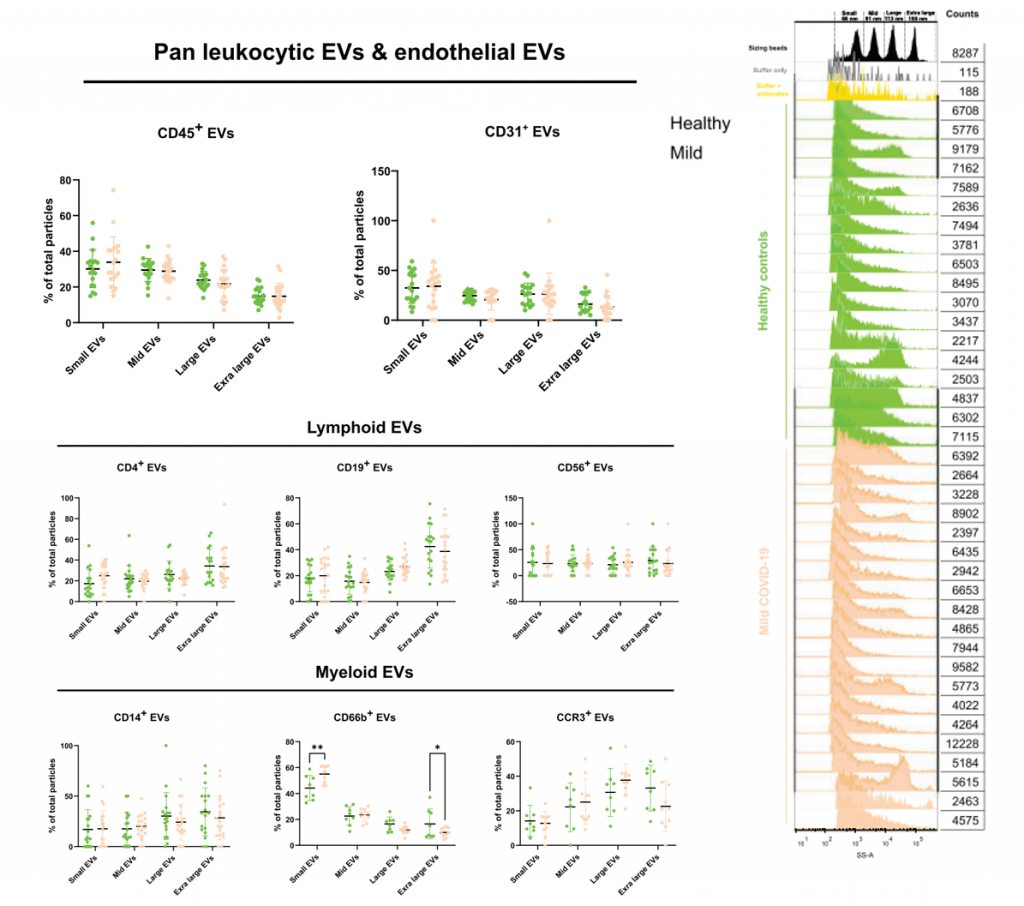
图2 新冠患者外泌体粒径分布和亚群分析
现有免疫细胞表型分析表明COVID-19患者的先天性免疫和获得性免疫均发生了大量改变,作者研究了经典的白细胞标志物CD45,发现与健康人相比,COVID-19患者的CD45阳性外泌体阳性率明显下降。随后作者监测了CD45随发病时间的变化情况,发现在感染新冠病毒3-13天时,CD45阳性的EVs比例明显下降,而在13天后CD45阳性外泌体的比例回升,这些都提示对感染COVID-19病毒13天前后进行外泌体分析的重要性。
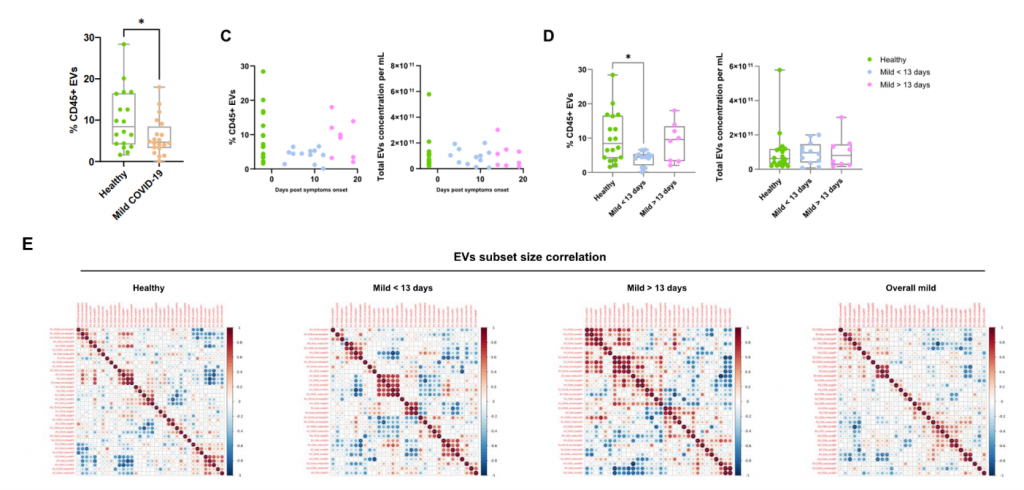
图3 不同感染时间的新冠患者蛋白表达相关性分析
有意思的是,CD45阳性外泌体的降低与另一项研究表明在新冠感染前期CD45阳性细胞减少互相验证,表明基于外泌体的检测方法可能具有高灵敏度和早期检测能力。通过皮尔逊相关系数分析发现,内皮组织分泌的CD31阳性外泌体主要集中在large和extra lage两个外泌体亚群,而small EVs主要表达CD14、CD19、CD56等蛋白,并且在13天前后趋势是相反的。这些数据都表明在新冠感染的早期,COVID-19病毒主要影响单核细胞、B细胞、NK细胞分泌的外泌体。
三、新冠外泌体Spike蛋白检测与起源
作者对新冠患者外泌体表面的Spike S1蛋白进行了检测,发现16例新冠感染者中有5例感染者Spike S1外泌体阳性率>1.75%,提示人血清中存在COVID-19特异性EVs,进而影响疾病进展。为了进一步确定Spike S1阳性外泌体的起源,作者用内皮细胞(研究发现与新冠相关)的蛋白标志物 CD31标记外泌体。发现与健康人相比,新冠感染者的Spike S1和CD31双阳性外泌体在感染前13天和后13天明显增加。这些数据表明,Spike S1阳性外泌体可能起源于新冠病毒感染的内皮组织细胞。为了更深入地了解血清EVs与疾病状态之间的关系,作者应用全队列人群血清EVs亚群水平的主成分进行分析,揭示了不同外泌体亚群与蛋白表达间的关系。


图4 新冠感染者外泌体Spike蛋白和不同发病时间相关性分析
本研究另外分析了COVID-19轻症患者血清EVs对健康外周血单核细胞的影响,发现COVID-19患者血清EVs能够以一种有针对性的方式影响B和T细胞应答,这可能有助于在COVID-19患者中观察到相应的免疫表型。
总结
作者利用nFCM对新冠患者的外泌体进行精细的亚群分析,表明或可通过检测血液外泌体在新冠感染的不同时间的变化情况,监控新冠感染进程。通过对外泌体进行蛋白标记,可确定血清中不同细胞来源的外泌体在新冠病毒感染期间的变化,开创性地对血液中外泌体的不同细胞来源进行精准分类和研究,以监测受影响的组织和疾病进展的严重程度。尽管与重症患者相比,COVID-19轻症患者的之间存在个体差异,且表型不那么明显,但这些探索性分析使得在传统临床方法的基础上,利用血清EVs来预测疾病状态成为可能!
NanoFCM可在单颗粒水平对EVs进行定性定量分析,区分EVs不同亚群,研究不同疾病或生理过程中EVs物质的变化,特别适用于血液等具有不同组织来源的EVs的表征,有望助力EVs在肿瘤、载药、免疫治疗等领域的研究!

附原文作者评论:NanoFCM具有超高的灵敏度和分辨率,可在单颗粒水平对EVs进行分析;可同时对EVs的粒径、浓度、蛋白进行定性定量表征,超越了目前使用的传统抗体包被磁珠的方法。
参考文献:
1.Yim K H W, Borgoni S, Chahwan R. Serum extracellular vesicles trace COVID-19 progression and immune responses[J]. medRxiv, 2022.