颠覆认知!LNP表面抗体不是越多越好,NanoFCM精准揭秘“黄金密度”!

单颗粒精度,让每个LNP的功能配体“开口说话”
抗体功能化修饰是脂质纳米颗粒实现mRNA精准递送的关键技术,尤其在in vivo CAR-T等前沿疗法中展现出巨大潜力。然而,一个长期困扰该领域的问题始终悬而未决:LNP表面到底需要偶联多少抗体,才能实现最佳递送?过去,我们只能通过投料比”进行经验性摸索,如同“黑箱操作”。但近日,日东电工株式会社(Nitto Denko Corporation)核酸药物事业部发表于《Nano Letters》的研究给出了颠覆性答案:配体密度与递送效率并非简单的正相关,而是呈现经典的“倒U型”关系。而揭示这一规律的核心利器,正是单颗粒纳米流式检测技术(NanoFCM)。本文将带您深度解析这项研究,看NanoFCM如何通过绝对定量,将LNP工程化从“经验掺混”推向“定量设计”的新纪元。
一、研究背景:当“精准递送”遭遇“定量盲区”
随着mRNA疗法从传染病疫苗拓展至癌症免疫治疗(如in vivo CAR-T),如何将mRNA精准递送至特定靶细胞成为核心挑战。将抗体(或纳米抗体VHH)偶联至LNP表面,是实现主动靶向的直接策略。然而,传统的表征方法存在致命的短板:
- “总量”≠“功能”:传统的BCA法或SDS-PAGE只能测定LNP悬液中的总蛋白量,无法区分哪些抗体是偶联在表面且具备活性的,哪些是包埋在内或失活的。
- “平均”≠“单颗粒”:即使测定了表面抗体的总量,也无法知晓每个颗粒上抗体的分布差异。大量空载或低载颗粒会严重拉低整体的靶向效率。
缺乏精准的功能配体密度表征手段,导致Ab-LNP的研发长期停留在“经验摸索”阶段,结果难以复现,机制无法阐明。
二、技术突破:NanoFCM——LNP功能配体的“精准计数仪”
在这项由日本Nitto Denko团队主导的研究中,研究者开发了一种基于VHH的LNP修饰平台,并创新性地引入了单颗粒纳米流式(NanoFCM) 来解决上述难题。他们建立了一套严谨的功能配体定量流程(图1e ):
- 构建探针:将Ab-LNP与荧光标记(AF488)的重组CD8蛋白孵育。只有表面活性的VHH能结合CD8蛋白,从而被“点亮”。
- 单颗粒检测:通过SEC柱去除游离探针后,利用NanoFCM对单个LNP颗粒进行双参数检测——侧向散射(反映粒径)和AF488荧光(反映结合的功能配体数量)。
- 绝对定量:借助标准微球分别进行粒径校准和ERF荧光校准,将散射信号转化为粒径,将荧光信号转化为绝对分子数,最终计算出每个LNP颗粒的配体密度(个/100 nm²)。
这一方法实现了三大飞跃:
- 从“总蛋白”到“功能配体”:只计数真正能结合受体的活性抗体。
- 从“群体平均”到“单颗粒异质”:揭示了不同LNP颗粒间配体密度的分布。
- 从“相对定量”到“绝对定量”:将密度作为可精确调控的工程参数。
三、关键发现:NanoFCM揭示的“黄金密度”与受体经济学
借助NanoFCM的精准定量能力,研究者得以构建连续的配体密度梯度,并系统性探究其与递送效率的关系,从而获得了一系列颠覆性发现。
1、线性调控与饱和平台
研究发现,VHH投料在0.008–0.25 mol%范围内时,表面功能配体密度呈线性增加。但当投料达到0.5 mol%时,密度进入平台期(图1j )。这个结果首次直观地证明了LNP表面存在“接枝饱和”现象,盲目增加投料只会造成浪费,这在过去是无法被清晰界定的。
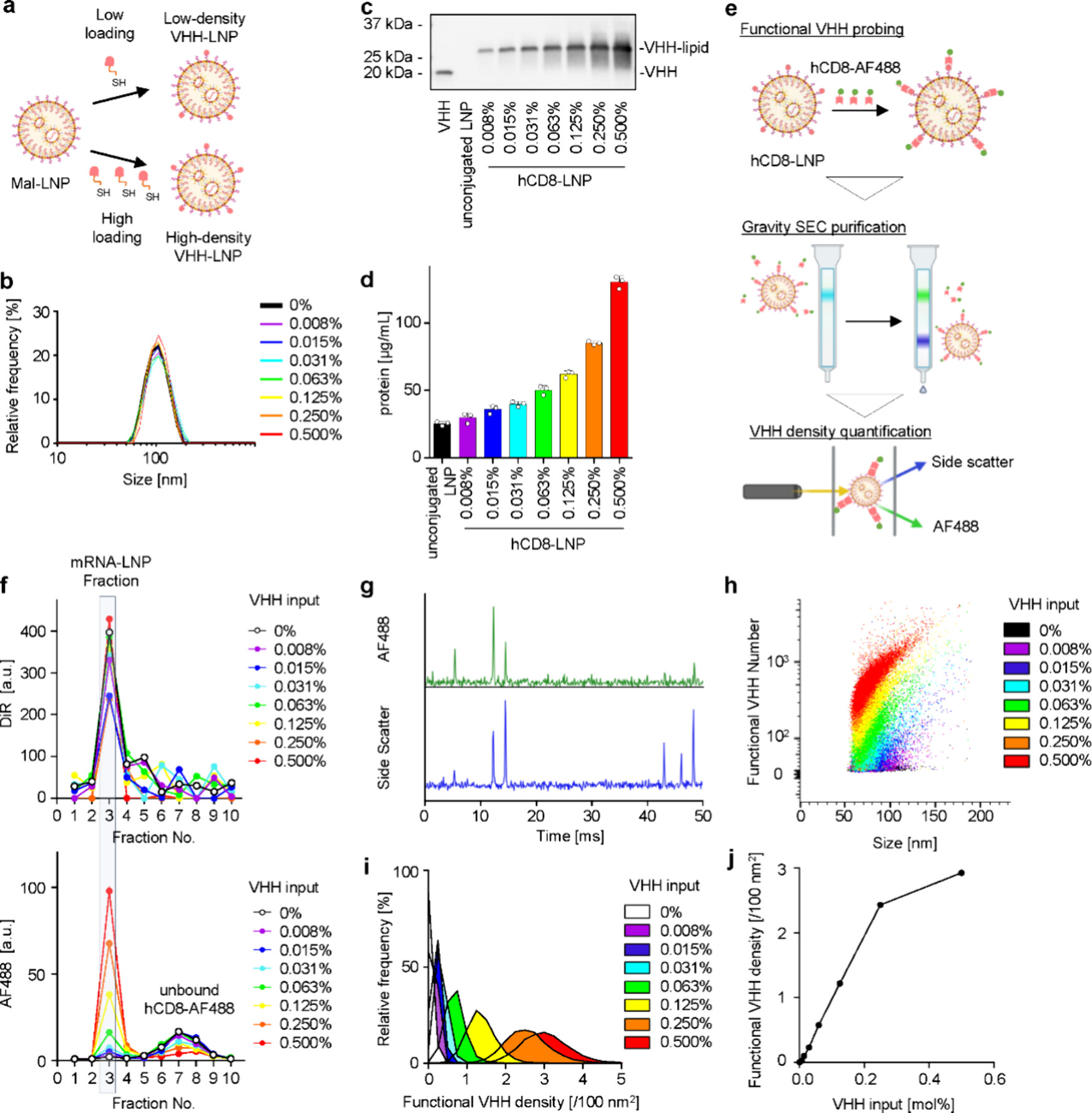
2、“倒U型”递送曲线
在明确功能密度后,研究者在体内外验证了递送效率。结果清晰地显示,CD8+ T细胞的转染效率与配体密度呈经典的“倒U型”关系(图2)。当配体密度约为 0.1 VHH/100 nm²时,体内 CD8⁺ T 细胞转染效率达到最高值 51.5%,且脱靶效应极低。无论是低于还是高于这个密度“黄金窗口”,递送效率均显著下降。
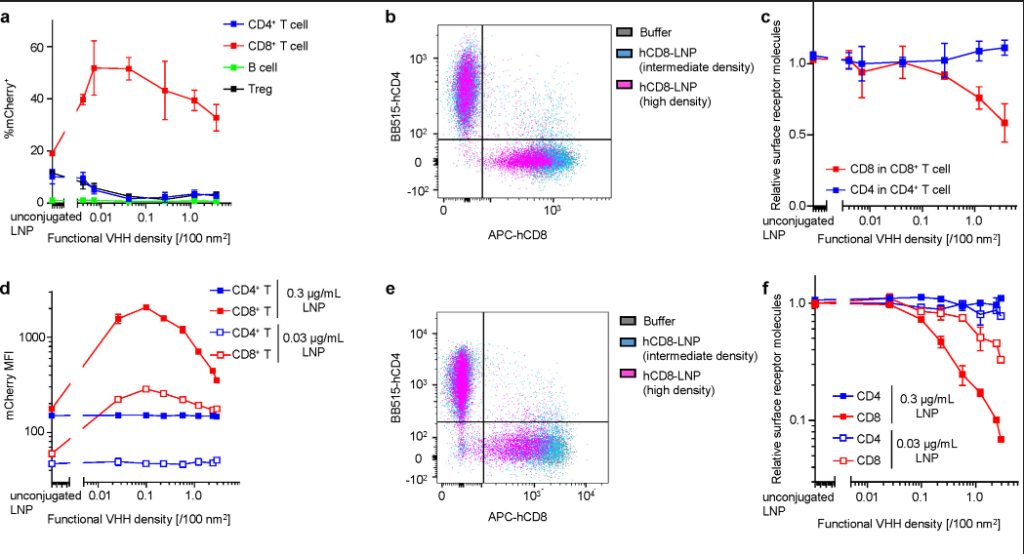
3、机制解析:高密度诱导受体降解
为什么高密度反而有害?NanoFCM定量结果结合后续流式细胞术和Western blot,揭示了深刻的“受体经济学”机制:
- 低密度:无法形成有效多价结合,难以驱动有效摄取。
- 最佳密度:实现多价结合与受体保留的平衡。
- 高密度:虽然增强了初始结合,但会诱导CD8受体快速内吞和降解(15-30分钟内CD8 受体信号下降59%,全长 CD8α 蛋白水平减少67%),导致后续LNP“无门可入”(图3)。
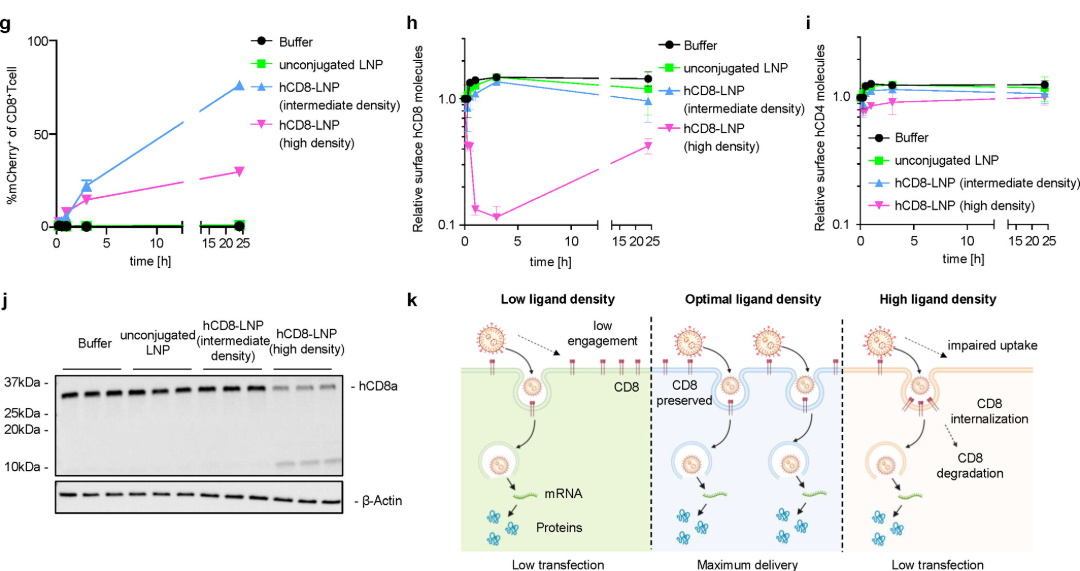
4、体内验证:极低剂量下的惊人疗效
研究团队将编码第二代临床级CD19 CAR(FMC63 scFv-CD28-CD3ζ)的mRNA负载于最优配体密度(0.1 VHH/100 nm²)的hCD8-LNP中,用于CD19 CAR‑mRNA递送,在Nalm6白血病小鼠模型中验证了其强大的抗肿瘤能力。结果显示,最优密度的CAR-LNP(0.1 mg/kg)治疗组实现近乎完全的肿瘤抑制,生物发光信号几乎消失;而对照组肿瘤则快速进展。治疗期间未观察到体重下降或其他毒性迹象,证实了良好的安全性(图4g-i)。
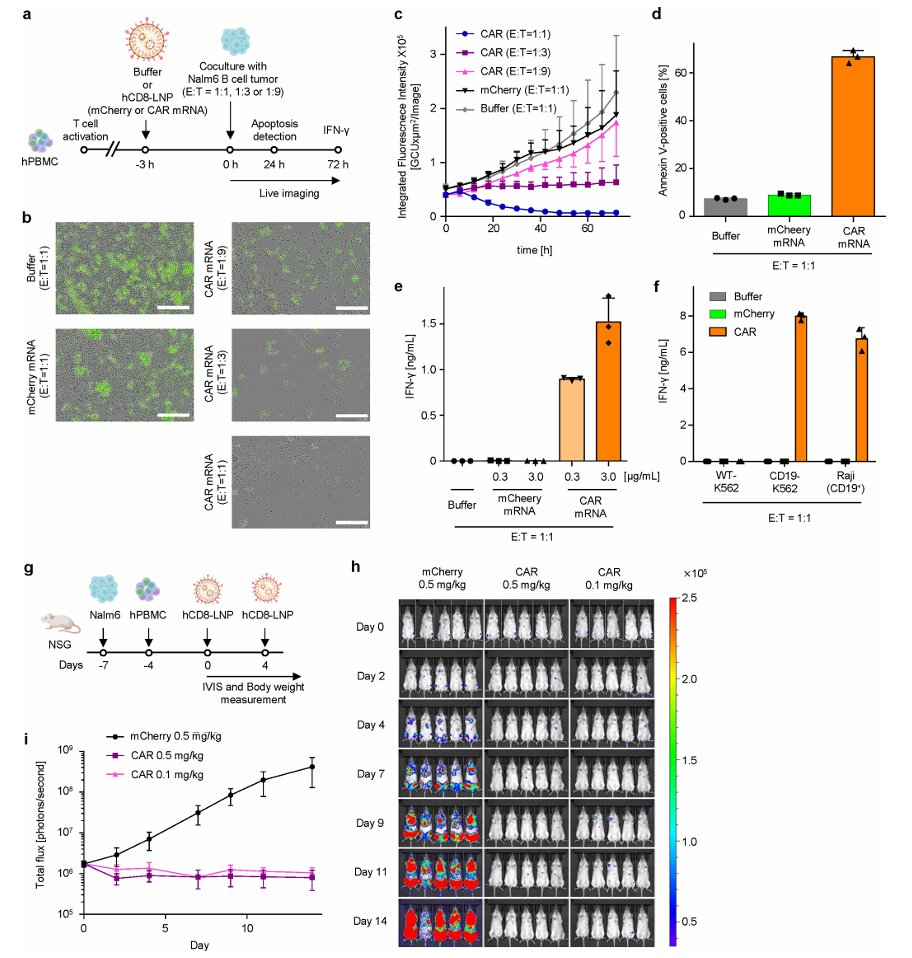
四、研究意义与转化价值
这项研究不仅带来了学术上的突破,更对LNP药物的临床转化具有里程碑意义。
- 建立理性设计范式:首次将表面功能配体密度作为独立、可量化的关键质量属性(critical quality attribute, CQA),为Ab-LNP的工程设计提供了首个定量基准(~0.1 VHH/100 nm²),终结了“经验主义”时代。
- NanoFCM成为质控基石:本研究证明了NanoFCM是唯一能实现功能配体精确定量的技术。它不仅是科研利器,更应成为靶向LNP药物工艺开发、批次放行和稳定性研究的标准质控工具。缺乏该工具,“黄金密度”将无从验证。
- 赋能极高效in vivo CAR-T:基于最优密度设计的CAR mRNA-LNP,在微克级剂量下即实现显著药效,为in vivo CAR-T疗法的临床转化提供了极具竞争力的候选方案。
五、展望:让每一个靶向LNP都“有据可依”
这篇《Nano Letters》文章是LNP靶向递送领域的一个转折点。它用严谨的数据告诉我们:在纳米药物的世界里,更精准的定量才能带来更深刻的理解,进而指导更理性的设计。而贯穿整个研究,从功能配体密度的线性调控、颗粒间异质性评估,到最佳递送窗口的精准定位,再到体内极致药效的验证,单颗粒纳米流式检测技术(NanoFCM)始终是核心数据来源。它让原本“看不见、数不清”的LNP表面,变得“可见、可数、可量化”。
作为这一技术的开创者和先行者,我们坚信,NanoFCM将成为下一代精准纳米药物研发不可或缺的“火眼金睛”。




