EVs荧光标记的机遇与挑战
Author: Mika Huang Date: February 10, 2022
细胞外囊泡(extracellular vesicles, EVs)在机体的多种生理病理过程中均发挥着重要作用,良好的结构稳定性、生物相容性及天然的转运能力使其成为理想的药物递送载体和治疗制剂。不管是在工业生产还是科学研究中,EVs的质量控制都至关重要,国际细胞外囊泡协会(international society for extracellular vesicles, ISEV)一直在努力推动和完善相关标准,如MISEV2014、MISEV2018以及即将发布的MISEV2022,同时工业界也试图确立适用于工业产品的质控标准。除了粒径、浓度等常规物理参数的检测,更重要的是对EVs的纯度、蛋白标志物、核酸以及载物等功能性分子进行表征,而内容物的定性定量分析通常需要通过荧光标记来实现。
近日Lonza集团的研发团队发表了题为“Opportunities and Pitfalls of Fluorescent Labeling Methodologies for Extracellular Vesicle Profiling on High-Resolution Single-Particle Platforms”的文章,作者分别利用高分辨单颗粒表征平台nFCM(NanoFCM)和F-NTA对EVs进行表征,探讨EVs荧光表征过程中面临的问题与挑战。文章对EVs纯度测定过程中染料的选择、蛋白标志物分析、RNA检测、复杂体系中EVs的表征等方面进行全面研究,指出在EVs综合表征中面临的问题与注意事项,供广大EVs研究者参考。

EVs纯度鉴定
首先,分别选取两种细胞膜染料和两种细胞质染料对EVs的纯度进行鉴定。nFCM结果显示,无论是细胞膜染料(CMG/CMR)还是细胞质染料(CFSE/CTR),EVs阳性颗粒的比例均高达90%左右,且EVs尺寸越大,结合的染料越多,荧光强度也越高。由于具备超高的散射和荧光灵敏度,nFCM证实了几种染料标记效率的一致性(图1)。同样的样品和染色方法用F-NTA检测,经CFSE标记的EVs阳性率为88%,与nFCM结果相当,而对于CMG染料标记,F-NTA测得的阳性颗粒比例只有32%左右,粒径分布显示F-NTA检测到的是大的EVs。这个案例提醒研究者对于EVs纯度分析不仅需要关注不同染料间的标记和检测效率问题,还需要关注表征平台的检测能力。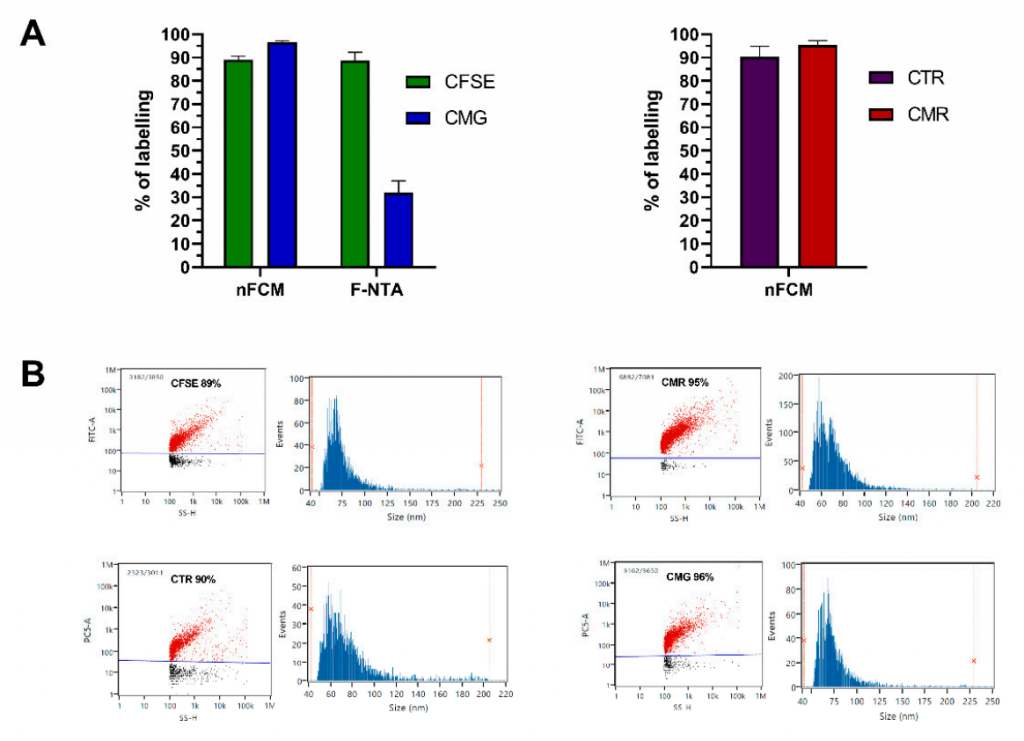
图1.不同染料标记EVs纯度的效率
EVs抗体选择和标记方法
在早期的推文中小编介绍过不同公司的抗体特异性存在差异重磅!安德森癌症中心用NanoFCM直筛外泌体特异性抗体!,抗体标签也是影响EVs标记效率的一个因素。该研究对比了PE、AF488、AF647、APC四种标签的CD9抗体,发现PE和AF488的标记比例优于AF647和APC,比例在50%左右;进一步选用PE和AF488两种标签的CD9、CD63和CD81抗体,发现在HT29和HEK293细胞系中不同标签抗体标记的效果没有显著差别(图2),说明在EVs蛋白标记过程中研究者需要格外关注抗体特异性、标签的选择对标记效率的影响。

图2.不同荧光标签对抗体标记效率的影响
除了抗体标签,未结合的抗体对EVs的阳性率也存在影响。文章对比了稀释法(Dilution)、超滤(UF)、尺寸排阻(SEC)三种方法对游离抗体去除效果和标记比例的影响。由于不涉及纯化过程,理论上稀释法对EVs的影响是最少的。nFCM结果显示三种方法得到的CD9、CD63、CD81阳性率基本一致,说明稀释法可以用来准确地测定EVs蛋白的比例,同时结果也证明UF和SEC纯化过程对EVs蛋白的阳性率没有影响(图3)。说明nFCM可通过稀释法测定EVs蛋白表达比例,省略超速离心去除游离抗体的操作,极大缩短操作时间,同时真实反映EVs蛋白表达比例和强度。
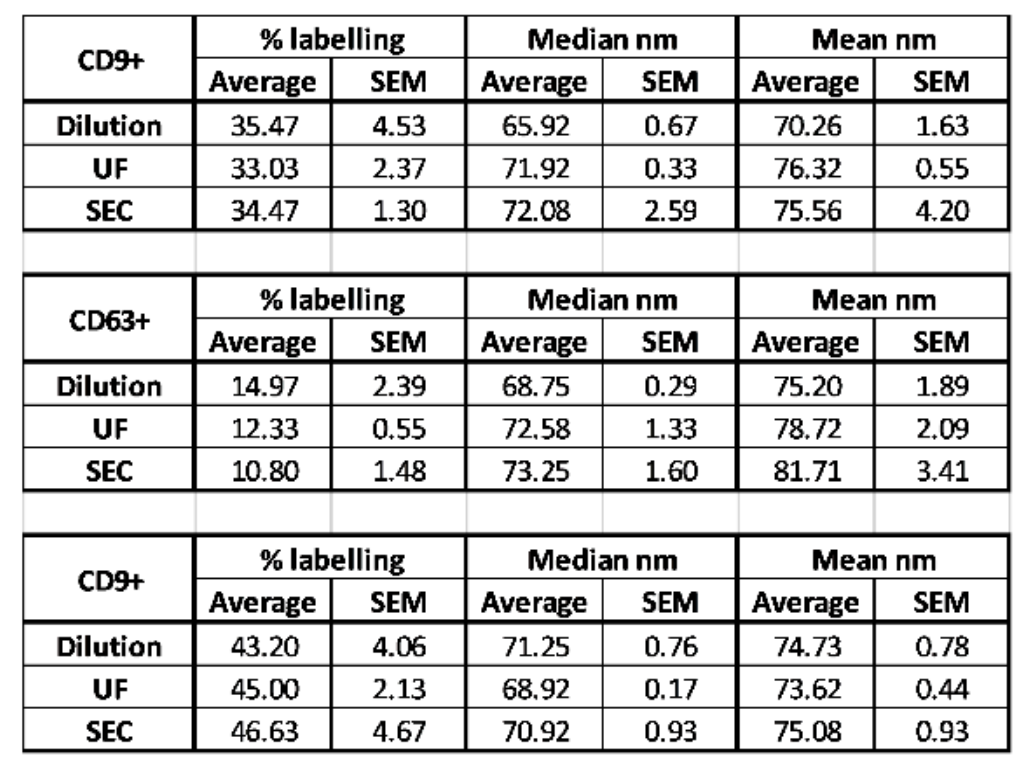
图3.nFCM测定游离抗体去除方法对标记比例的影响
细胞上清中EVs的直接检测
前面介绍的案例都是基于EVs纯品的分析,杂质颗粒含量非常低,对测定结果的影响相对较小。进一步对较复杂的细胞上清(CCM)进行直接检测,作者指出对于EVs纯品和CCM样品,nFCM的结果令人惊讶的一致,CFSE与CMG阳性率例均在90%左右,与超离纯化的 HT29 EVs样品结果一致,说明nFCM平台既适用于纯的EVs样品,也可用于细胞上清样品中EVs的直接检测,具有广泛的应用场景;而在F-NTA平台,CFSE与CMC对于HT29细胞上清EVs标记阳性率分别为33%和27%,作者解释称可能是由于CCM样品复杂的成分导致F-NTA的检测存在差异;对于蛋白比例检测,3种EVs蛋白marker总比例高达188.5%,远远超过100%,文章指出可能是F-NTA荧光的灵敏度高于散射,大量小颗粒的散射信号未检出,导致比例高于100%。

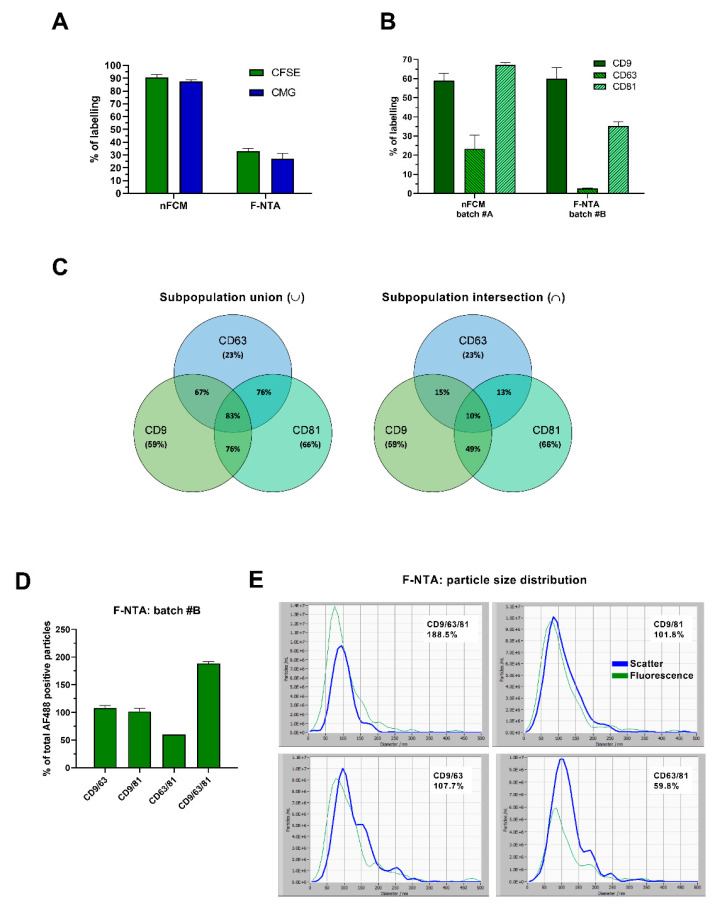
图4.CCM样品EVs纯度和蛋白比例测定
与F-NTA相比,nFCM还可以利用多色荧光标记策略对sEV亚群进行表征。为研究EVs的抗体单标和双标之间是否相互影响,作者选取CD9-AF488和CD81-PE分别进行单独标记和双标,对比标记比例的变化。结果表明这两个蛋白之间,不管是单独标记或双标,阳性率差异不显著;另外,用EVs染料CTR和CD81同时标记EVs,发现所有CD81阳性的EVs的CTR均呈现阳性,说明CD81阳性的颗粒,均是EVs!(图5)。nFCM可以准确识别抗体标记的所有EVs,并且确认抗体阳性率的准确性。
图5.EVs抗体单标和双标的影响
结论
综上,Lonza集团的研发团队对EVs荧光标记过程中的各项指标进行综合对比,对EVs纯度测定过程中染料的选择、蛋白标志物分析、复杂体系中EVs的表征等进行研究,对工业生产中EVs的质量控制提供了新思路和新方法。
作者肯定了nFCM用于EVs检测的准确性和灵敏度,提出EVs纯度表征方法,初次采用CD9/63/81几种抗体的混合物验证EVs的纯度,并对细胞上清中的EVs进行直接检测,得到了跟EVs纯品相一致的结果。另外作者指出nFCM对于EVs荧光检测具有更高的灵敏度和稳定性(图6),nFCM可在单颗粒水平对EVs的散射和荧光进行同时检测,单次采样即可实现蛋白与EVs(或蛋白间)的“共定位”分析,是EVs质量控制中不可或缺的工具。![]()

图6.文中关于nFCM的评价
附录:
Lonza Walkersville(龙沙集团)是全球CDMO龙头企业,一家以生命科学为主导,在生物化学、精细化工、功能化学等行业均处于领先地位的全球性跨国公司,具有一百多年历史,总部位于瑞士巴塞尔。
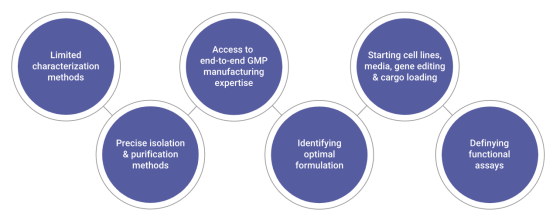
图7.Lonza集团EVs工作流程图(图片来源:Lonza官方网站)
Lonza目前已采购3台NanoFCM,分别用于EVs研发、生产质控和CRO项目,致力于EVs大规模生产、纯化和表征,后续将应用于EVs载药领域。2021年11月,Lonza收购了Codiak公司位于马萨诸塞州Lexington的外泌体生产基地,正式成为Codiak管线的战略制造合作伙伴。届时Lonza将借助Codiak的高通量外泌体生产技术向第三方提供服务,并开发先进的外泌体产品,助力细胞与基因治疗产业。
参考文献:
- Fortunato D, Mladenović D, Criscuoli M, et al. Opportunities and Pitfalls of Fluorescent Labeling Methodologies for Extracellular Vesicle Profiling on High-Resolution Single-Particle Platforms[J]. International Journal of Molecular Sciences, 2021, 22(19): 10510.
- https://www.lonza.com/
- https://www.lonza.com/news/2021-11-02-13-01



